Persontilpasset risikovurdering av prostatakreft ved bruk av dyplæring og digital patologi
En av de største utfordringene innen behandling av prostatakreft er å finne frem til hvilke pasienter som trenger umiddelbar behandling, og hvilke som trygt kan gå inn i et behandlingsregime som kalles «aktiv overvåkning».
I dette prosjektet brukes digital patologi og kunstig intelligens (KI) for å utvikle et mer presist verktøy for risikovurdering på diagnosetidspunktet. Ved å bygge videre på en dyplæringsmodell som opprinnelig ble utviklet for kirurgisk fjernede preparater, skal prosjektet tilpasse denne metoden til diagnostiske vevsprøver (biopsier). Målet er å bedre kunne vurdere svulstens aggressivitet når kreften først oppdages. Hensikten er å redusere unødvendig overbehandling ved å forbedre utvelgelsen av pasienter til aktiv overvåkning, samtidig som man sikrer raskere behandling for pasienter med aggressiv sykdom.
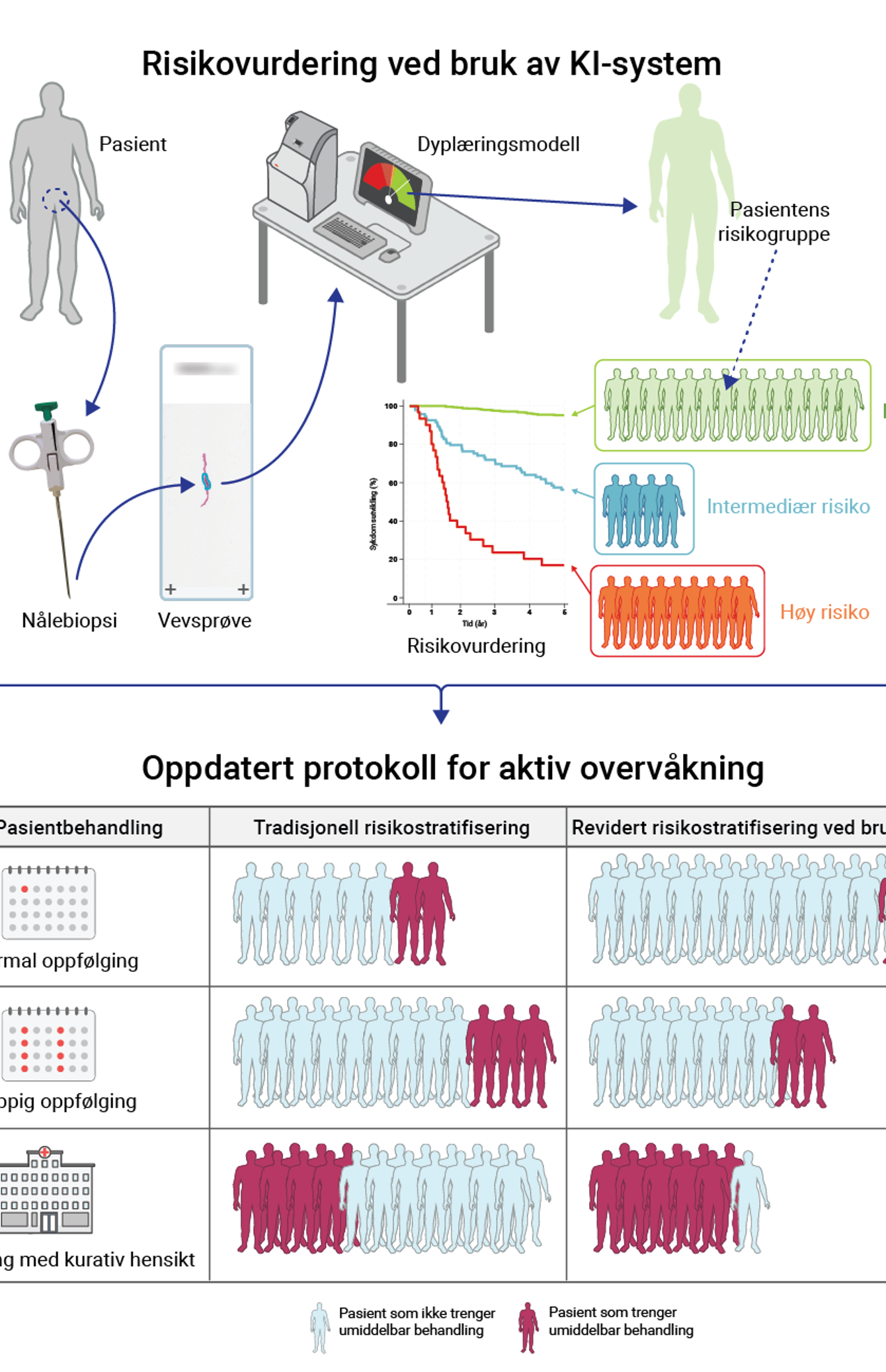
Dette prosjektet utvikler et nytt, KI-basert verktøy for persontilpasset risikovurdering av pasienter med prostatakreft. Ved å bruke dyp læring til å analysere diagnostiske vevsprøver (biopsier), kan teknologien nøyaktig forutsi kreftens hissighet allerede på diagnosetidspunktet. Målet er å løse et av de største dilemmaene i moderne kreftbehandling: å redusere unødvendig overbehandling gjennom tryggere bruk av aktiv overvåkning, samtidig som man sikrer rask, livreddende behandling for pasienter med aggressiv sykdom.
Dilemmaet i dagens kreftbehandling
Prostatakreft er en global helseutfordring og den vanligste kreftformen blant menn i Norge, med over 5 200 nye diagnoser årlig. Selv om PSA-testing og MR-veilede biopsier har forbedret tidlig oppdagelse av sykdommen, har de også ført til et betydelig klinisk dilemma: hvordan man skal balansere fordelene ved tidlig diagnose opp mot risikoen for overbehandling.
Gap mellom forskning og klinisk praksis
For å kunne ta tryggere beslutninger om hvem som bør opereres og hvem som kan overvåkes, trengs det bedre prognostiske verktøy på diagnosetidspunktet. I dagens kreftforskning utvikles nye biomarkører ofte ved å studere store mengder vev fra hele prostatakjertler som er fjernet kirurgisk. Men når den faktiske beslutningen om behandling skal tas, har legen kun tilgang til små diagnostiske nålebiopsier, som ofte utgjør mindre enn 0,2 % av prostatavolumet.
Fordi svulster i prostata er heterogene – det vil si at biomarkører er ujevnt fordelt i svulsten – kan små nålebiopsier gi et ufullstendig bilde av kreftsykdommen. Verktøy utviklet på store kirurgiske preparater er derfor ofte ikke direkte overførbare til biopsiprøver, noe som skaper et betydelig gap mellom forskning og klinisk nytteverdi.
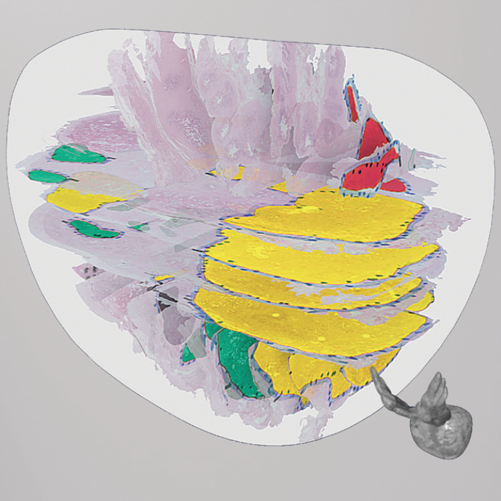
Kunstig intelligens som problemløser
Dette prosjektet bruker dyplæring for å tette gapet mellom forskning og klinikk ved å tilpasse en eksisterende modell (DoMore-v1-PCa), opprinnelig utviklet ved Institutt for kreftgenetikk og informatikk. Modellen forutsier pasientforløp ved å analysere digitale bilder av vanlige vevssnitt fra opererte pasienter. Den identifiserer subtile endringer i vevets utseende som er knyttet til hvor aggressiv sykdommen er – endringer som ikke fanges opp av tradisjonelle kliniske mål. Målet er å videreutvikle og skreddersy denne teknologien slik at den også fungerer på små nålebiopsier.
KI-modellen trenes og testes på et omfattende datasett med nesten 7 000 digitaliserte vevsprøver fra pasienter behandlet ved Oslo universitetssykehus og sykehusene i Vestfold, Vestre Viken og Telemark. Dette inkluderer prøver fra både opererte pasienter og pasienter i aktiv overvåkning.
En innovativ tilnærming til klinisk beslutningsstøtte
Det overordnede formålet er å integrere de KI-analysene med tradisjonelle kliniske målinger for å skape et sikkert og helhetlig verktøy for beslutningsstøtte. Dette vil gi leger et tryggere og mer presist grunnlag for å skille mellom pasientgrupper, noe som betyr færre pasienter i den usikre mellomrisikokategorien. På sikt vil dette bidra til å redusere overbehandling, sikre bedre pasientutfall og fremme en mer effektiv ressursbruk i helsetjenesten.
Prosjektet er finansiert av Helse Sør-Øst i perioden 2026 til 2029.